小激活RNA:走向新型治疗药物和临床治疗的发展
引言
小干扰RNA(siRNA)和microRNA(miRNA)是基因表达的关键调节因子,被认为是小型双链RNA(dsRNA)分子[1–3]。它们被加载到Ago蛋白上,形成活性的Ago-RNA复合物,该复合物在转录和转录后水平上调节基因表达[4,5]。多项研究表明,dsRNA主要通过染色质修饰或翻译抑制来抑制基因表达[6–9]。一种新型的小型dsRNA,称为小激活RNA(saRNA),能够通过靶向一些基因的启动子序列而不是抑制基因表达,这被称为“RNA激活”(RNAa)[10–13]。saRNA长度为21核苷酸,在哺乳动物中以Ago2依赖的方式起作用,类似于RNAi [11]。尽管最初的报告表明通过靶向启动子区域的合成dsRNA可以激活基因表达,但更近期的研究证实RNAa是一种在从线虫到人类等不同真核生物中存在的进化保守机制[14,15]。与小型双链激活RNA一样,已经证实一些miRNAs通过靶向启动子序列和/或UTR中的AU丰富元件来激活基因表达[11,16,17]。多项独立研究表明,一类新的激活RNA可以由天然反义转录本(NATs)生成[14–16]。反义转录本,称为长非编码RNA,是从蛋白编码基因座的相反DNA链上转录的,与相应的编码RNA互补。它们是功能元素,以组织特异性方式表达,并且通常富含[17]。最近的报告表明,反义转录本通过多种转录和转录后机制调节它们的正向(蛋白编码)伙伴[18,19]。虽然大多数反义转录本抑制相应的正向基因表达,但它们也可以被视为saRNAs的靶点[13,15]。值得注意的是,阻断正向(mRNA)和反义转录本(形成天然双链)的相互作用和/或通过siRNAs或单链寡核苷酸(antagoNATs)破坏反义转录本,导致基因座特异性转录去抑制和基因上调,可能通过激活RNAi机制[14–16]。除了启动子序列被认为是saRNAs的主要靶点外,通过小RNA片段激活基因的作用可能发生在任何存在反义转录本的基因组区域。尽管saRNAs提供了巨大的优势,但仍然存在一些关键挑战,限制了这些尖端治疗方法的发展。最显著的挑战包括siRNA稳定性低、在血流中的降解和被吞噬,以及非特异性靶向效应(表1)。纳米颗粒介导的递送系统可以为克服这些问题打开一种新的途径。
在这篇综述中,我们介绍了小激活RNA在治疗应用方面的最新进展和挑战。
表1. 使用saRNAs作为治疗方法的优缺点。
- 优势:
· 有效的基因激活 · 对基因转录的局部特异性激活,包括难以药物靶向的目标 · 制造容易 · 成本效益高 · 低毒性 · 易于大规模生产 · 免疫原性低
- 缺点:
· 细胞摄取差 · 对RNase降解高度敏感 · 肾脏清除 · 重复给药 · 非特异性靶向效应 · 激活Toll样受体
小激活RNA参与神经基因的局部诱导
小激活RNA介导的基因座特异性激活已在神经细胞中进行了研究。根据许多研究,有两种基因座特异性激活的模型,即以启动子为靶标的双链RNA激活和天然反义破坏,导致染色质结构的变化[8,14,15,20]。几项研究表明,内源性小激活RNA通过靶向启动子序列在神经元中选择性激活基因表达[21,22]。Kuwabara等人报道了一个大约20个碱基对的神经特异性dsRNA,其中包含NRSE(神经元限制性沉默元件)序列。这个序列被定义为NRSE/RE1,位于神经元特异基因的启动子区域,并由神经限制性沉默因子/RE-1沉默转录因子(NRSF/REST)识别,在非神经元细胞中导致神经特异基因抑制。在神经发生的早期阶段,NRSE dsRNA诱导含有其启动子中NRSE/RE1序列的基因的表达。事实上,作为内源性激活RNA的非编码dsRNA与NRSF/REST机制相互作用并调节其功能。通过这一过程,神经干细胞可以分化为神经元和胶质细胞[21]。细胞介导的大脑修复受到移植细胞的存活率低和分化为神经元细胞效率低的困扰[23]。Diodato及其同事使用预miRNAs(作为激活RNA)来增加Emx2的表达,Emx2是一个人类顶盖转录因子,调节多种发育机制,如大脑皮层的发育。他们的结果显示,Emx2的转录激活可以导致神经元前体细胞的延迟分化、自我更新和死亡减少[24]。Fimiani及其同事报告了在大脑中外源saRNA介导的基因激活[22]。合成的saRNA诱导Foxg1转录因子的表达,这是一个关键的调控因子,用于皮质-脑功能的发育。在人类中,Foxg1等位基因的重复和删除分别导致West和Rett综合症[25]。作为Rett综合症的前瞻性RNAa治疗,通过对小鼠新生儿进行脑室内注射saRNA,已成功诱导了神经细胞中Foxg1基因的表达[22]。 NATs破坏是另一种可行的基因座特异性激活机制,具有巨大的治疗潜力。例如,Modarresi等人研究了大脑源性神经营养因子(BDNF)基因座的天然反义转录本的调控作用[14]。BDNF是神经营养因子家族的成员,对神经成熟、可塑性、记忆过程和分化至关重要[26–31]。有趣的是,在单链寡核苷酸(术语antagoNAT)或siRNAs降解天然反义转录本后,体内外均证实了BDNF表达的基因座特异性诱导[14]。通过在神经球中抑制BDNF-AS后,内源性BDNF表达诱导了神经前体细胞的分化。与这些体外实验相对应,在小鼠中脑室内注射BDNF-antagoNAT9后,体内BDNF mRNA和蛋白表达也被诱导。在BDNF诱导的情况下,似乎通过调节表观遗传修饰,即减少BDNF座位的H3K27me3抑制标记,应用了一种RNAa机制。使用RNAa系统短暂诱导神经营养因子表达被提出作为多种神经系统障碍的药理学方法,因为在不同的神经退行性和神经发育性障碍中观察到神经营养因子表达降低[14]。
脊髓性肌肉萎缩症(SMA)是神经肌肉障碍的另一个例子[32]。功能性生存运动神经元蛋白(SMN)的不足表达与疾病严重程度相关,导致出生后肌肉无力[33–35]。多项治疗努力集中在增加SMN表达上[32]。d’Ydewalle等人在SMN(SMN-AS)座上鉴定了一种天然反义转录本,通过表观遗传修饰转录抑制SMN表达。重要的是,抗反义转录本在患者衍生的细胞中或在体内SMA小鼠模型的中枢神经系统中敲低抗反义转录本,都会诱导SMN转录活性,改善小鼠的存活率,表明了SMA的新型治疗靶点[36]。
我们认为,将RNAa治疗用于各种神经退行性和神经发育性障碍的临床转化的下一步是开发新型的药物递送系统。
小激活RNA参与心脏基因的基因座特异性诱导
已报道了小激活RNA介导的基因转录的基因座特异性激活在心血管细胞中[37–39]。在所有报道的研究中,通过小型双链RNA或小型发夹RNA(shRNA)靶向启动子区域导致心血管基因的转录激活,为治疗策略打开了道路。例如,通过shRNA靶向血管内皮生长因子(VEGF)的启动子区域导致转录激活,暗示了治疗心肌梗塞的策略[37]。最近已经证明,通过靶向反义转录本可作为心脏发育关键参与者,如细胞周期依赖性激酶9(Cdk9)座的替代RNA激活系统[15,16]。Cdk9与特异性环素结合形成异源二聚体,Cyclin T/Cdk9,也被称为正转录延伸因子b(P-TEFb)[40–42]。P-TEFb通过磷酸化羧基末端结构域(CTD)激活聚合酶II转录机制[43,44]。因此,Cdk9主要参与转录调控,在几个分化途径中发挥关键作用。此外,Cdk9通过与p300/GATA4复合物的相互作用调节心脏特异基因,包括Nkx2.5、Anf和ß-Myh,特别参与心脏分化[45]。此外,我们最近发现Cdk9通过调节miRNA-1表达在心肌细胞中调控凋亡,miRNA-1对心脏分化至关重要[46–48]。因此,Cdk9的合成和活性可能在转录和转录后水平上受到严格调控。在这方面,至少有三种非编码RNA参与Cdk9的调控[16]。在正常人类心肌细胞的情况下,通过与7SK非编码RNA的相互作用,在蛋白水平上抑制了Cdk9的活性,通过肌肉特异性miRNAs,特别是miR-1和miR-133,抑制了其翻译水平[46,49,50]。我们最近报道了Cdk9座的RNA控制的第三种模式[15]。具有与转录本同源序列的22bp小非编码RNA分子导致Cdk9的转录激活。有趣的是,已经鉴定了与基因的最3'和5'区域互补的NATs。事实上,将短的单链同源转录片段与反义转录本杂交为转录激活提供了信号。Argonaute蛋白和内源性反义转录本对于转录激活的要求表明,激活的单链小RNA是由RNAi机制加工的[51,52]。与siRNA敲低类似,通过感应性寡核苷酸电穿孔后的反义转录本干扰可能代表RNAi机制激活的二级现象。这种激活随后可能导致基因座上表观遗传修饰的改变,从而诱导Cdk9转录,正如对其他几个基因的描述[1,53]。作为RNA激活在Cdk9座的功能结果,通过电穿孔与感应性寡核苷酸的ES细胞观察到心脏分化潜能的增加。有趣的是,将经过RNA程序化的ES细胞注入野生型囊胚中,在体内特异性地促进心脏发育,表明短暂的RNA激活系统足以在细胞中创建心脏分化的“记忆”,可能代表应用于再生医学中的RNA-细胞重编程的新工具。
小激活RNA:癌症治疗的新见解
最近,由于其有望选择性靶向先前难以药物靶向的基因和基因表达调节器,基于RNA的治疗在癌症治疗中引起了更多关注。与主要靶向正义转录本的RNAi不同,作为一种替代且具有前景的新治疗策略,RNAa可以通过靶向反义转录本或启动子区域以自然方式激活基因表达[13,54–56]。在癌症中通常受抑制的肿瘤抑制基因可以通过saRNA靶向,增强转录激活并恢复正常细胞表型。
saRNAs可以通过诱导细胞周期停滞、细胞衰老、抑制增殖、诱导凋亡、抑制转移和逆转多药耐药性来发挥其抗癌效应(图1)。尽管包括E-钙粘附蛋白、NKX3-1、Wt1和P53在内的多个抑癌基因已通过这种方法被诱导,但在多个肿瘤和细胞系中,p21是最受研究的RNAa介导的基因激活的肿瘤抑制基因[10,57–62]。P21是细胞周期的负调节器,在癌症中很少突变,因此代表了小RNA激活癌症治疗的关键靶标。在这方面,通过靶向启动子区域重新激活p21基因抑制了细胞的存活能力和增殖速率,同时诱导细胞凋亡并使肺癌细胞对化疗药物敏感,为癌症治疗提供了一种新方法[59,60,63]。
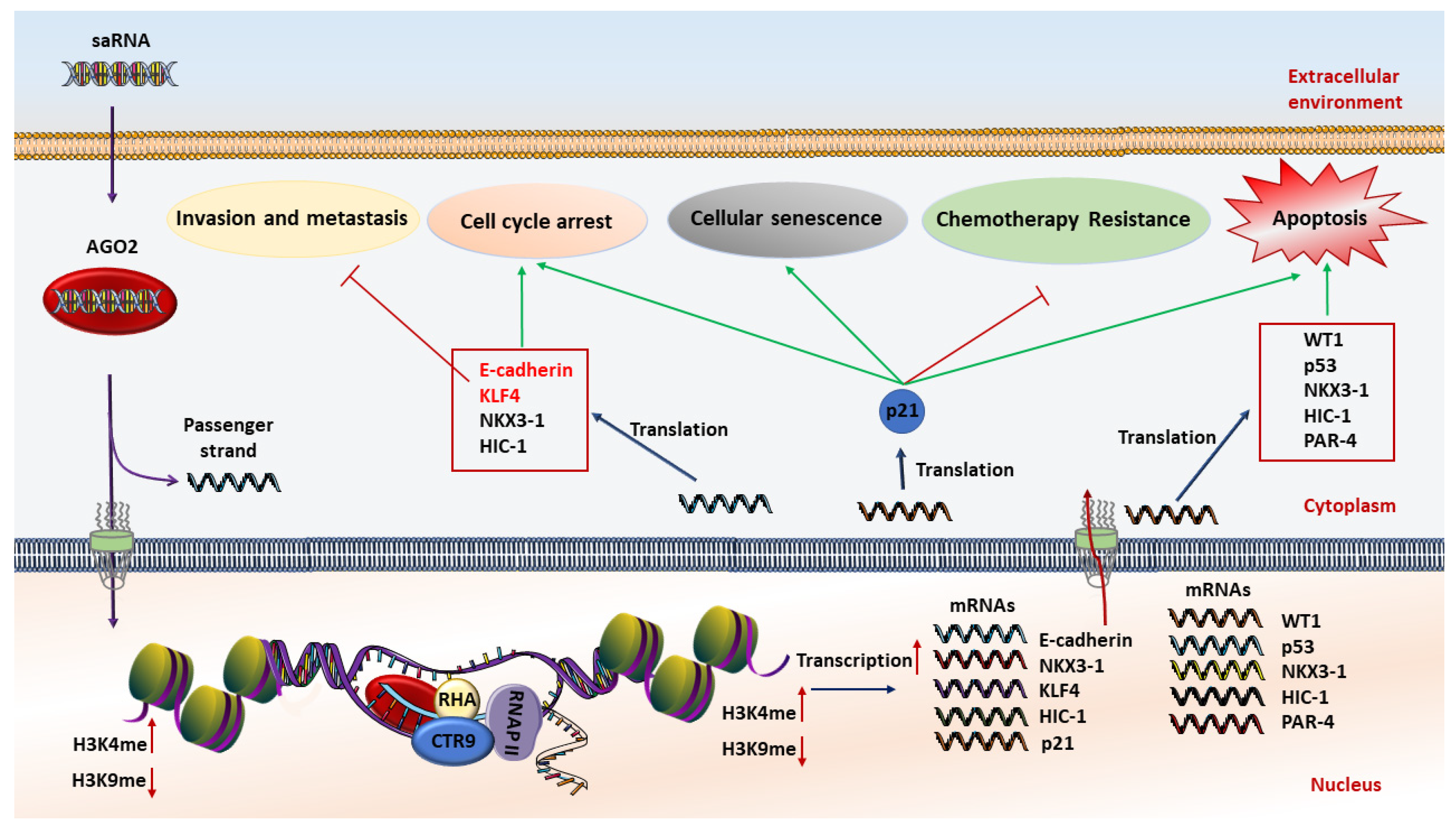
图1. saRNA(小激活RNA)基治疗的抗癌机制的示意图。首先,saRNA被加载到AGO2蛋白上。然后,AGO2分离载体链。之后,saRNA引导链和AGO2的复合物穿越核膜,并与感兴趣基因的启动子序列相互作用,通过甲基化H3K4和/或去甲基化H3K9增加转录。肿瘤抑制基因的表达水平得以恢复,导致凋亡诱导、化疗抵抗逆转、侵袭和转移的抑制、细胞周期停滞以及细胞衰老。
朝着新型小激活RNA药物的发展
在过去的几年中,针对不同疾病进行了大量的临床研究,评估了小激活RNA作为治疗方法的潜力(详见表2和附表S1)。
由于它们可能涉及人类疾病,已经付出了巨大努力来开发应用RNAa策略的新治疗药物。例如,美国的两家公司,RNAa Therapeutics和OPKO-CURNA,正在研究基于RNA激活的治疗方法。值得注意的是,mipomersen,一种靶向载脂蛋白B的寡核苷酸,在2013年1月获得了FDA的批准,但在欧洲药品管理局小组中获得了负面意见[90]。由于其高效性、特异性、基因座特异性功能、正确细胞靶向、小分子大小和低毒性,RNA激活分子作为有前途的药物正在积极研究中[10,91]。传统上,通常需要外源DNA构建来进行异位基因表达。除了排除调控元素的外源DNA构建外,由于需要病毒载体进行基因传递,这些系统在临床中存在问题。包括宿主基因组完整性、构建过程的繁琐性以及先前报告的各种负面免疫反应等多种病毒基因疗法的限制和不良副作用[92–95]。作为成熟物质传递的一部分,RNAa系统通过靶向启动子区域或通过天然反义破坏,以在没有外源DNA的情况下以基因座特异性的方式激活内源靶向基因表达,提供了一种更自然的方法和更安全的基因治疗方法。此外,RNAa在天然细胞环境中提供了内源诱导,导致具有适当修饰的正确加工的蛋白质。值得注意的是,在通过天然反义破坏进行基因激活的情况下,源自正义转录本(mRNA)的短寡核苷酸可以充当激活RNA [15],这更安全、更自然,并且不会激活免疫反应。
为了提高saRNAs的药物特性和体内应用潜力,必须采取两个步骤。首先,必须开发新型基于纳米颗粒的药物递送系统,以增加药物在靶向组织中的积累,并解决saRNAs治疗应用中上述挑战。迄今为止,已经开发了不同的递送系统来传递saRNAs。最近,基于脂质的纳米颗粒(LNPs)引起了全球关注。LNP基于的递送系统面临严重的限制,如毒性、低热力学稳定性、包封效率低以及泄漏等挑战[96]。为了克服这些限制,提出了各种策略。使用灵活的、非离子性、亲水性聚合物(如PEG)对递送系统进行表面修饰,被提出作为解决血清蛋白opsinization问题的强有力策略[97,98]。此外,表面用可生物降解的纳米聚合物(如PEG)修饰可以用来降低纳米颗粒的毒性[99]。为了增加P21的表达,使用新型PEG修饰的脂质纳米粒子将2'-氟修饰的P21 saRNA(dsP21-322-2'F)传递到原位膀胱癌小鼠模型中。结果显示,尿道上皮摄取显著增加,肿瘤明显缩小[80]。配体,核酸酸配体,可用于有针对性的药物递送,因为它们可以根据其序列形成特定的三维结构。Yoon及其同事合成了PDAC特异性的2'-氟吡咯烷基RNA配体(2'F-RNA)- P19和P1,用于将saRNA有针对性地传递到植入了PANC-1和AsPC-1的小鼠体内。在两个肿瘤小鼠模型中静脉注射配体–C/EBPα saRNA后,与用吉西他宾治疗的小鼠相比,肿瘤生长显著受到抑制[84]。
发展有效的saRNA治疗的第二步依赖于定制saRNA的位点特异性化学修饰。例如,阻断载体链的5'-OH和对2'骨架的修饰(即2'-OMe,2'-Fluoro和锁核酸酸)已被证明可以减少其非靶向潜力,并分别提高内切酶抵抗力和血清稳定性[55,58,100]。对于被指定为antagoNAT的单链治疗性寡核苷酸,化学修饰不仅促进代谢稳定性和靶向特异性,还将寡核苷酸的长度最小化以提高细胞摄取。在这种情况下,具有每端三个锁核酸酸(LNA)替代和磷酸硫酸酯修饰的16-核antagoNAT寡核苷酸,也称为gapmer [101],已在体内研究中使用[14,102–105]。除了通过化学修饰来改善稳定性和特异性之外,寡核苷酸的有针对性和高效体内传递对于基于RNA的治疗也至关重要。在目前正在研究的各种方法中[106–109],基于脂质的配方是系统性或局部saRNA传递的最有前景的载体[100,110,111]。正在测试RNAa基药物的几项临床试验通常使用脂质载体[112,113]。考虑到关于RNAa基于基因座特异性激活的新策略的增加的知识,明显存在着发展基于这种创新方法的新治疗药物和临床治疗的科学和商业兴趣。脂质纳米粒子配方的核苷酸修饰RNA最近被引入作为Covid-19疫苗,支持脂质基传递的高效性、安全性和RNA疗法的效果[114,115]。
结论和未来展望
基于RNAa的药物在过去几年中引起了极大的关注,因为它们在治疗各种疾病方面具有很高的潜力。然而,传递挑战减缓了这一新型治疗药物类别的临床转化。酶消化、低细胞摄取、差劲的内体逃逸、非靶效应和从血流中快速清除已经迫使不仅对RNAa分子进行优化,而且对传递系统进行优化。已经设计和开发了许多非病毒传递系统,用于传递基于RNAa的治疗系统。基于纳米颗粒的传递系统具有高度功能化和靶向能力、易于大规模开发等优势,使其成为医学应用中有前途的传递系统。例如,多项研究表明,对不同材料(如PEI)进行PEG化可以增强它们的循环时间,减少溶血和血清opsinization。RNA分子的化学修饰标志着这些尖端RNA治疗的发展新时代。然而,由于可能发生严重的副作用和功能降低,这些修饰可能受到限制,这是亟需解决的问题。
由于制药公司将提供的巨大大规模合成能力,RNAa基治疗的未来应用将因药物传递载体的发展进展、非靶问题的减少而显着提升。使用RNAa与化疗药物的组合策略也可能成为不同类型疾病的新的强大治疗模式。